|dr Justyna Knapik-Kowalczuk|
W obliczu pandemii wirusa SARS-CoV-2 wiele osób zastanawia się, jak długo trwa proces powstawania nowego leku. Droga od zidentyfikowania choroby do stworzenia, zarejestrowania i wprowadzenia na rynek nowego leku jest niezwykle długa. Jeśli wykryta zostanie przyczyna schorzenia, wynalezienie, przebadanie, sprawdzenie oraz weryfikacja leku na to schorzenie trwa około 12–14 lat. Jak podaje amerykańska Agencja Żywności i Leków FDA, jeśli uzasadniają to okoliczności, czas ten można znacząco skrócić poprzez pominięcie etapu badań klinicznych. Niemniej jednak nawet „przyspieszony” tryb wprowadzania nowych substancji leczniczych trwa około 5–6 lat. Dzieje się tak, ponieważ zaproponowana do leczenia substancja musi być nie tylko skuteczna na dane schorzenie, ale również bezpieczna dla pacjenta.
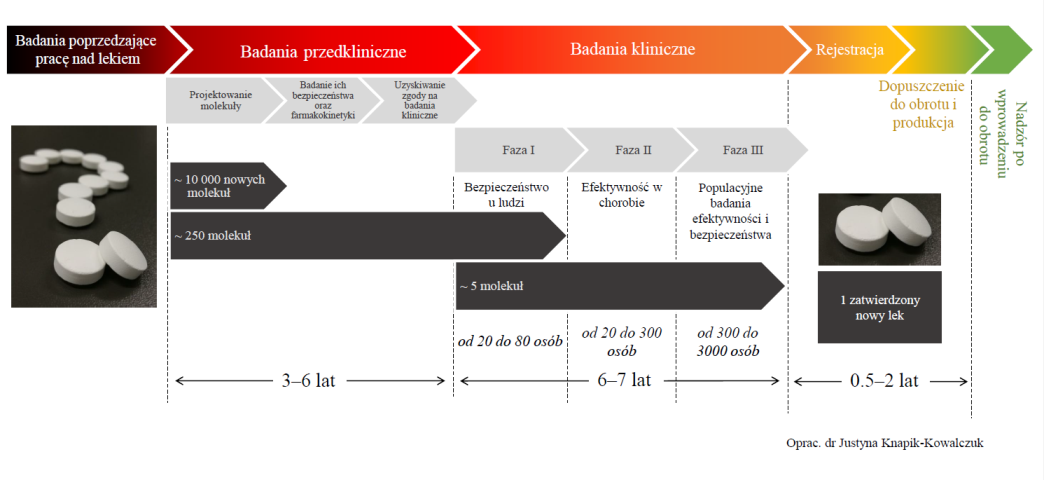
Standardowo proces wprowadzania nowych leków odbywa się zgodnie z poniższym opisem.
Grafika prezentująca kolejne etapy opracowywania nowych leków (oprac. dr Justyna Knapik-Kowalczuk):
Odkrycie „celu”
Po wykryciu nowej choroby pierwszym krokiem do stworzenia leku jest zidentyfikowanie naturalnie istniejącej struktury komórkowej lub molekularnej zaangażowanej w patologię, którą nowo powstały lek powinien zmodyfikować. Może to na przykład być białko z mikroorganizmu powodującego chorobę. Krok ten oczywiście poprzedza etapy bezpośrednio związane z rozwojem leku, lecz jest niezbędny do znalezienia efektywnego na dana chorobę leku. Dzięki temu etapowi zaczynamy rozumieć chorobę, dowiadujemy się, gdzie należy „celować” aby ją zwalczyć i bazując na tym możemy przystąpić do kroków związanych z odkrywaniem leku.
Badania przedkliniczne (trwają zwykle od 3 do 6 lat)
- projektowanie molekuł
Proces poszukiwania nowego leku na wybrany cel danej choroby zazwyczaj składa się z wysokowydajnych badań przesiewowych podczas których testuje się ogromną ilość rozmaitych substancji chemicznych lub układów biologicznych pod kątem ich zdolności do modyfikacji celu. Substancje te są projektowane, symulowane przy pomocy odpowiednich programów komputerowych, syntezowane oraz odpowiednio oczyszczane. Jeśli okaże się, że cząsteczka (lub układ biologiczny) modyfikuje „cel” w sposób, który pomaga zwalczać chorobę naukowcy przekazują ja do kolejnego etapu badań koncentrując na niej swoja uwagę. W tym kroku wybraną cząsteczkę poddaje się wielu delikatnym modyfikacjom mającym na celu poprawę bezpieczeństwa oraz efektywności działania takiego leku. Średnio tworzy się i testuje około 10 000 nowych modyfikacji wybranej z badań przesiewowych substancji. Finalnie spośród wszystkich powstałych substancji do dalszych badań wyłanianych jest jedyne kilka procent najlepiej rokujących molekuł.
- badania bezpieczeństwa oraz farmakokinetyki kandydatów na leki
W późnych badaniach przedklinicznych wybrany kandydat na lek jest poddawany dalszym badaniom laboratoryjnym tym razem jednak celem jest potwierdzenia jego bezpieczeństwa dla ludzi i sprawdzenie jego farmakokinetycznych właściwości (np. odpowiedniej absorpcja lub metabolizm w ludzkim ciele). Aby potwierdzić biologiczne działanie danego leku przeprowadzane są, z nadzwyczajna starannością, badania na zwierzętach. Podkreślić należy, że badania te odgrywają bardzo ważną rolę w badaniach nad nowymi lekami. Pomimo tego, iż bardzo dużą część badań można przeprowadzić w laboratorium lub wysymulować przy pomocy komputera, skomplikowane mechanizmy chorobowe bardzo często mogą być w pełni zrozumiane tylko dzięki badaniom przeprowadzonych na zwierzętach. Poza tym istnieją regulacje prawne mówiące o tym, że zanim lek zostanie testowany na ludziach musi pozytywnie przejść badania na zwierzętach. Oczywiście możliwie redukuje się liczbę uczestniczących w takich badaniach zwierząt do niezbędnego minimum. Co więcej każde badania nad zwierzętach przeprowadza się po uzyskaniu odpowiedniego pozwolenia. Takie pozwolenie wydawane jest tylko wtedy, kiedy naukowo dowiedziono ich wysokiej potrzeby (obowiązuje zasada 3R przy badaniach nad zwierzętami).
Uzyskanie zgody na badania kliniczne
Aby rozpocząć badania z udziałem pacjentów, konieczne jest złożenie wniosku o wydanie pozwolenia na prowadzenie badania klinicznego. W Polsce wnioski kieruje się do Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych oraz właściwej komisji bioetycznej. (pierwszą odpowiedź otrzymuje się do 60 dni od złożenia wniosku).
Badania kliniczne
Badania kliniczne składają się z trzech etapów, każdy z nich jest zaprojektowany w taki sposób, aby zapewnić/potwierdzić bezpieczeństwo danego leku oraz jego efektywność w walce z chorobą (trwają około 6-7 lat)
- pierwsza faza badań klinicznych – najczęściej jest przeprowadzana na niewielkiej grupie (od 20 do 80 osób) zdrowych ochotników. Jej celem jest potwierdzenie/zbadanie bezpieczeństwa, toksyczności, farmakokinetyki oraz farmakodynamiki badanej substancji. W przypadku niektórych leków w tej fazie badań mogą uczestniczyć pacjenci w zaawansowanym stadium choroby,
- druga faza badań klinicznych – substancja podawana jest grupie od 20 do 300 chorych pacjentów, aby ocenić kliniczną skuteczność (efektywność) terapii, ustalić optymalną dawkę substancji, kontynuować testowanie jej bezpieczeństwa dla ludzi oraz określić wywoływane przez nią skutki uboczne (warto podkreślić, że mogą być one inny w porównaniu do zdrowych ochotników z pierwszej fazy),
- trzecia faza badań klinicznych – w tej fazie substancje podaje się wyselekcjonowanej, stosunkowo dużej (od 300 do 3000 lub więcej) grupie ludzi grupie. Faza ta na celu sprawdzenie/potwierdzenie efektywności (skuteczności) nowej terapii oraz monitorowanie skutków ubocznych. Pozwala stworzyć dokumentację potwierdzającą/wyjaśniającą jak podawać (zażywać) daną substancję, aby była ona bezpieczny. Jest to bardzo istotne, ponieważ jak powtarzał Paracelsus (zwany ojcem medycyny nowożytnej) Wszystko jest trucizną, decyduje tylko dawka.
Rejestracja
Aby wprowadzić nowy lek na rynek musi on oczywiście zostać zarejestrowany. Rejestruje się go na podstawie przygotowanego dossier zawierającego wszystkie informację, w tym wyniki z przeprowadzonych dotychczas badań. Dokumenty te wraz z wnioskiem składa się do Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych. Decyzję w sprawie dopuszczenia do obrotu produktów leczniczych wydaje Prezes Urzędu. Jeśli lek ma być dopuszczony również na pozostałą część Europy lub na cały Świat dodatkowe procesy rejestracyjne są wymagane. Pamiętajmy różne warunki klimatyczne (temperatura, wilgotność) panują w różnych obszary świata, dlatego inne badania są wymagane przy rejestracji leku np. w Polsce i w Indiach.
Wprowadzenie nowego leku na rynek farmaceutyczny
Po wydaniu pozytywnej decyzji rejestracyjnej nowy lek może zostać wprowadzony do obrotu.
Kontrola
Po wprowadzeniu leku na rynek firma farmaceutyczna jest zobligowania do kontrolowania uzyskiwanych efektów leczenia i zdawania z tego corocznych raportów – ten proces można nazwać czwartą fazą badań klinicznych.
Warto podkreślić, że tak długi czas „powstawania” nowego leku nie wynika z faktu, że firmy farmaceutyczne i naukowcy zwlekają z prowadzeniem badań. Wręcz przeciwnie, ich poszukiwania i działania są niezwykle intensywne.
Czas ten jest niezbędny, aby zminimalizować ryzyko wprowadzenia na rynek substancji niebezpiecznej dla ludzi. Świetnymi przykładami niebezpiecznych substancji, które zdecydowano się kiedyś wprowadzić na rynek są talidomid oraz heroina.
Talidomid jako lek o działaniu przeciwwymiotnym, przeciwbólowym oraz usypiającym sprzedawano bez recepty w latach 1957 – 1961 kobietom, których ciąża przebiegała z powikłaniami. Po czterech latach sprzedaży udowodniono, że ten, potencjalnie fantastyczny, preparat ma silne działanie teratogenne (tj. powoduje nieodwracalne uszkodzenia płodu). Ofiarami kilkuletniej obecności tego leku na rynku było około 15 tys. ludzkich płodów. Drugą wyżej wspomnianą niebezpieczną substancją, która w 1898 roku została zarejestrowana jako lek przez firmę Bayer jest heroina. O tym silnie uzależniającym półsyntetycznym opioidzie mówiono, że nie powodowała uzależnień oraz jest fantastyczny w leczeniu kaszlu. Stąd też zalecano heroinę do leczenia astmy, gruźlicy i zapalenia oskrzeli. Ciekawostka jest sama nazwa tej substancji powstała na bazie opinii pacjentów, którzy wielokrotnie powtarzali, że po zażyciu tej substancji czują się jak herosi – czują się heroicznie. Po wielkiej fali krytycznych doniesień na temat faktycznego działania heroiny w 1913 roku Bayer zaprzestał produkcji tej substancji. Dziś jako lek, pod bardzo surowymi zasadami wydawania, zarejestrowana jest jedynie w kilku państwach.